Pesquisadores da Johns Hopkins Medicine relatam que um novo estudo financiado pelos Institutos Nacionais de Saúde está ajudando a promover uma nova abordagem potencial para o tratamento da doença de Alzheimer. O foco é uma proteína no cérebro que produz um gás pequeno, mas importante.
Uma proteína chamada cistationina γ-liase, ou CSE – mais conhecida por produzir sulfeto de hidrogênio, o gás que cheira a ovo podre – parece desempenhar um papel fundamental na forma como a memória é formada. As descobertas vêm de experimentos em ratos geneticamente modificados, de acordo com o líder do estudo, Bindu Paul, MS, PhD, professor associado de farmacologia, psiquiatria e neurociência na Escola de Medicina da Universidade Johns Hopkins.
Pesquisa, publicada Anais da Academia Nacional de CiênciasO objetivo é compreender melhor como funciona esta proteína e se o aumento da sua atividade pode ajudar a proteger as células cerebrais e a retardar doenças neurodegenerativas como o Alzheimer.
O sulfeto de hidrogênio pode proteger as células cerebrais
Estudos anteriores sugeriram que o sulfeto de hidrogênio pode ajudar a proteger os neurônios em camundongos. No entanto, o gás é altamente tóxico, tornando inseguro a sua entrega diretamente ao cérebro. Em vez disso, os cientistas estão tentando descobrir como manter com segurança os pequenos níveis naturalmente presentes nos neurônios.
Novas descobertas mostram que ratos sem a enzima CSE desenvolvem problemas de memória e aprendizagem. Esses camundongos também apresentaram aumento do estresse oxidativo, danos ao DNA e baixa integridade da barreira hematoencefálica – características comumente associadas à doença de Alzheimer, disse Paul, autor correspondente do estudo.
Com base em anos de pesquisa
O trabalho atual baseia-se em pesquisas anteriores lideradas por Solomon Snyder, MD, D.Sc., D.Phil., professor emérito de neurociência, farmacologia e psiquiatria. Em 2014, seu A equipe relatou que a CSE apoia a saúde cerebral em ratos com doença de Huntington. Os pesquisadores usaram ratos sem a proteína CSE, desenvolvida pela primeira vez em 2008, quando a proteína foi adicionada ao Função vascular e regulação da pressão arterial.
Em 2021, o grupo descobriu que a CSE não funcionava adequadamente em ratos com doença de Alzheimer e que injeções muito pequenas de sulfeto de hidrogênio ajudavam a preservar a função cerebral.
Estes estudos anteriores concentraram-se em ratos com mutações genéticas adicionais ligadas a doenças neurodegenerativas. As pesquisas mais recentes distinguem o papel do CSE.
“Este trabalho recente indica que a CSE por si só é um ator importante na função cognitiva e pode fornecer um novo caminho para o tratamento da doença de Alzheimer”, disse o co-autor Snyder, que se aposenta da Faculdade de Medicina Johns Hopkins em 2023.
A perda de memória está associada à deficiência de CSE
Para entender melhor como a CSE afeta a memória, os cientistas compararam ratos sem a proteína com ratos normais usando a mesma cepa desenvolvida em 2008. Eles testaram a memória espacial (a capacidade de lembrar instruções e seguir pistas) usando uma configuração chamada Labirinto de Barnes.
Neste experimento, os ratos aprendem a escapar de uma luz forte encontrando um abrigo escondido. Aos dois meses de idade, os ratos normais e aqueles sem CSE tiveram desempenho semelhante, encontrando o abrigo em três minutos. Mas aos seis meses, os ratos deficientes em CSE lutam para encontrar rotas de fuga, enquanto os ratos normais continuam a ter sucesso.
“A perda de memória espacial indica um início progressivo de doença neurodegenerativa que podemos atribuir aos danos da CSE”, disse a primeira autora Suvarna Chakraborty, pesquisadora do laboratório de Paul.
Mudanças cerebrais refletem a doença de Alzheimer
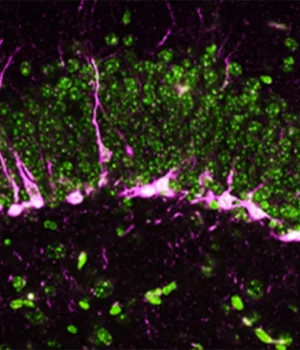
Os pesquisadores examinaram como a ausência de CSE afeta o cérebro no nível celular. O hipocampo, região importante para o aprendizado e a memória, depende da formação de novos neurônios. A interrupção desse processo é uma característica conhecida das doenças neurodegenerativas.
Usando métodos bioquímicos e analíticos, a equipe descobriu que as proteínas envolvidas na neurogênese estavam reduzidas ou ausentes em camundongos sem CSE.
Usando um microscópio eletrônico de alta potência, os cientistas observaram danos estruturais no cérebro desses ratos. Eles encontraram grandes rupturas nos vasos sanguíneos, indicando danos na barreira hematoencefálica, outra característica da doença de Alzheimer. Além disso, os neurônios recém-formados tiveram dificuldade em chegar ao hipocampo, onde normalmente contribuem para a formação da memória.
“Os camundongos deficientes em CSE foram comprometidos em vários níveis, o que associamos aos sintomas da doença de Alzheimer”, disse o co-autor Sunil Yamuna Tripathi, pesquisador do laboratório de Paul.
Rumo a novos tratamentos para Alzheimer
De acordo com os Centros de Controle e Prevenção de Doenças dos EUA, a doença de Alzheimer afeta mais de 6 milhões de pessoas nos Estados Unidos e o número continua a aumentar. Atualmente, nenhum tratamento demonstrou consistentemente parar ou retardar a doença.
Os investigadores dizem que visar a CSE e a sua produção de sulfeto de hidrogénio pode fornecer um novo caminho para o desenvolvimento de terapias destinadas a proteger a função cerebral e a retardar a progressão da doença.
Contribuidores de financiamento e pesquisa
O apoio financeiro para esta pesquisa foi fornecido pelos Institutos Nacionais de Saúde (1R01AG071512, P50 DA044123,1R21AG073684, O1AGs066707, U01 AG073323, AG077396, NS101967, NS837, NS837, Departamento de Defesa). (HT94252310443), American Heart Association, AHA-Allen Initiative in Brain Health and Cognitive Impairment, Solve ME/CFS Initiative, Catalyst Award da Johns Hopkins University, Valor Foundation, Wick Foundation, Department of Veterans Affairs Merit Award (S0565) Department of Medical Affairs Veterans Center, Mary Alice Smith Fund for Neuropsychiatry Research, Lincoln Neurotherapeutics Research Fund, Gordon and Avi Safran Neuropsychiatry Fundo; e o Fundo Leonard Krieger da Fundação Cleveland.
Além de Paul, Snyder, Chakraborty e Tripathi, os colaboradores incluem Richa Tyagi e Benjamin Orsburn, da Johns Hopkins; Edwin Vazquez-Rosa, Kalyani Chaubey, Hisashi Fujioka, Emiko Miller e Andrew Pieper da Case Western University; Thibaut Vignon e Milos Filipovic do Instituto Leibniz de Ciências Analíticas na Alemanha; Sudarshana Sharma, do Hollings Cancer Center; Bobby Thomas, do Derby Children’s Research Institute e da Universidade Médica da Carolina do Sul, e Zachary Weil e Randy Nelson, da Escola de Medicina da Universidade de West Virginia.