Uma equipe de pesquisa liderada pelo cientista da Universidade Autônoma de Barcelona (UAB), David Reverter, identificou o mecanismo molecular que controla a divisão celular bacteriana. A descoberta revela como a proteína MraZ se liga ao agrupamento de genes dcw para regular este processo. Os resultados são publicados Comunicação da natureza.
A divisão celular é essencial para todos os organismos vivos e depende da atividade coordenada de muitas proteínas e elementos reguladores. Na maioria das bactérias, as instruções para esse processo são organizadas dentro de um grupo de genes conhecido como operon dcw. Este cluster contém a informação genética necessária para produzir proteínas responsáveis pela divisão celular e pela construção da parede celular bacteriana.
Como o operon dcw ativa genes de divisão celular
Os genes neste cluster são ativados por proteínas conhecidas como fatores de transcrição. Essas proteínas se ligam a um pedaço específico de DNA chamado promotor, que marca onde começa a transcrição. Este ponto inicial aparece logo antes do primeiro códon (a unidade básica da informação genética) que sinaliza o início da sequência da proteína.
Um desses fatores de transcrição é o MraZ, que é o primeiro gene no operon dcw em todas as bactérias. Quando o operon MraZ é ativado, os genes dentro do cluster produzem proteínas necessárias para a divisão da bactéria. Assim, o MraZ atua como um regulador chave que controla a atividade dos operons que governam a divisão celular na maioria das espécies bacterianas.
Imagem dos mecanismos moleculares da divisão bacteriana
Um grupo de pesquisa da UAB liderado por David Reverter, professor titular do Departamento de Bioquímica e Biologia Molecular e pesquisador do Instituto de Biotecnologia e Biomedicina da UAB (IBB-UAB), descobriu o mecanismo detalhado por trás desta regulamentação. A equipe usou métodos avançados de biologia estrutural, incluindo cristalografia de raios X e microscopia crioeletrônica.
Essas técnicas permitem aos cientistas determinar como o fator de transcrição MraZ se liga ao promotor do operon dcw nas bactérias. Micoplasma genitalium. Este microrganismo é frequentemente utilizado em pesquisas de laboratório porque contém um genoma extremamente pequeno.
Visão em nível nuclear do DNA de ligação à proteína MraZ
A região promotora do operon dcw consiste em quatro segmentos repetitivos, ou “caixas”, de seis nucleotídeos cada. Estas sequências repetitivas de DNA desempenham um papel fundamental na regulação transcricional.
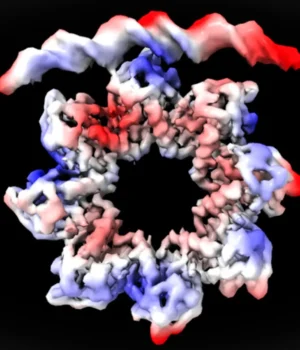
Ao examinar o sistema com microscopia crioeletrônica, os pesquisadores conseguiram observar a interação entre a proteína MraZ e as bases de DNA dessas quatro caixas repetidas em resolução quase atômica. Suas observações mostraram que o MraZ deve passar por uma mudança estrutural para se ligar com sucesso ao operon.
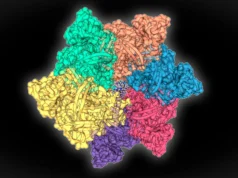
“Esta é uma observação surpreendente. A proteína MraZ é um octâmero composto por oito subunidades idênticas que se unem em forma de donut, mas com uma curvatura que nunca permite que caiba nas quatro ‘caixas’ do promotor. Porém, para controlar a divisão celular, vemos como o donut se quebra e se deforma de tal forma que as quatro subcaixas de David podem se juntar. David explica.
Um grande avanço na compreensão da divisão celular bacteriana
Visualizar diretamente como o MraZ interage com o DNA promotor que inicia a divisão celular representa um avanço significativo. Até agora, os investigadores que estudam este sistema basearam-se principalmente em experiências bioquímicas e modelos computacionais para prever como o processo funciona.
Segundo Reverter, o mecanismo regulador identificado neste estudo é provavelmente difundido entre as bactérias. “É universal para a maioria das bactérias, pois todas as proteínas MraZ são muito semelhantes, têm a mesma estrutura de octâmero e as sequências de DNA dos promotores dos operons que controlam a divisão celular também são semelhantes”, concluiu Reverter.
Cooperação internacional por trás do estudo
A pesquisa foi liderada pela equipe de David Reverter do Instituto de Biotecnologia e Biomedicina e do Departamento de Bioquímica e Biologia Molecular da UAB. O trabalho foi realizado em colaboração com o Serviço de Microscopia Síncrotron e Crioeletrônica da ALBA do Instituto de Genética e Biologia Molecular e Celular de Estrasburgo, França.